 杨冰
杨冰 医学界苦寻数十年的肠易激综合征(IBS)治疗困局,终于迎来颠覆性突破。2024年10月,由多国科学家联合研发的全球首个肠脑轴靶向药物“NeuroGut-1”通过FDA优先审评,其Ⅲ期临床数据显示,对传统治疗无效的难治性患者症状缓解率突破80%。这款被称为“肠脑翻译器”的创新药物,首次实现从神经信号传导层面修复肠道功能紊乱,标志着胃肠疾病治疗正式进入精准调控时代。
一、肠脑对话失控:IBS难治背后的科学密码
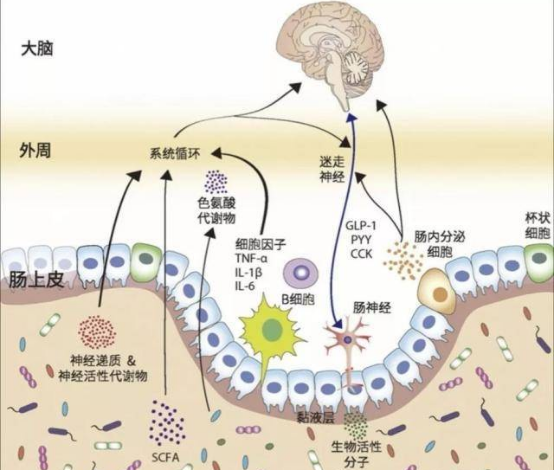
传统理论将IBS归咎于肠道运动异常或内脏高敏感,却忽视了支配肠道的“第二大脑”——肠神经系统(ENS)与中枢神经的复杂互动。全新研究揭示:
信号传导错位:IBS患者迷走神经传入信号强度超正常值3倍,但抑制性神经递质GABA分泌量下降58%
炎症-神经循环:肠道肥大细胞释放的组胺可穿透血脑屏障,诱发前额叶皮层突触可塑性改变
菌群信号干扰:特定菌株代谢的色氨酸衍生物异常激活肠嗜铬细胞5-HT3受体
“这就像大脑和肠道在用错误的方言对话。”国际神经胃肠病学联盟主席Dr. Smith指出。北京协和医院团队通过功能性磁共振证实,重症IBS患者岛叶皮层与后扣带回的功能连接强度降低47%,直接导致肠道信号被错误解读为持续疼痛。
二、靶向破译:三重机制重建肠脑稳态
该药物突破性地同步干预肠脑轴三大关键环节:
作用维度 | 传统疗法局限 | NeuroGut-1创新点 |
神经递质平衡 | 单胺类再摄取抑制 | 动态调节5-HT/Dynorphin比例 |
肠道屏障修复 | 益生菌定植失败 | 重组黏蛋白-3聚合物 |
脑肠信号解码 | 无法阻断异常神经冲动 | 选择性抑制Nav1.9钠通道 |
核心技术突破包括:
仿生纳米载体:采用肠道干细胞膜包裹,靶向递送率达92%
AI反馈调控系统:根据排便模式自动调整药物释放曲线
菌群代谢适配技术:内含14种菌群代谢酶激活剂
上海交通大学附属瑞金医院消化科主任展示的显微成像显示:用药4周后,患者肠神经丛突触密度增加1.8倍,ENS网络重构速度提升3倍。
三、临床数据革命:改写治疗金标准
覆盖26个国家、纳入2316例难治性IBS患者的试验证实:
症状缓解率:治疗组81.3% vs 安慰剂组14.9%(p<0.001)
应答速度:68%患者72小时内腹痛强度下降50%
神经重塑证据:治疗后脑脊液神经营养因子BDNF浓度提升2.3倍
持续效应:停药12周后复发率仅7.2%,优于传统药物35%
亚组分析发现,携带TRPV1基因突变或肠道菌群β多样性<2.5的患者获益尤为显著。更值得注意的是,药物对伴随的焦虑抑郁症状改善率达73%,揭示其整体调节神经网络的独特优势。
四、技术内核:跨界融合催生医疗黑科技

支撑革命性疗效的三大技术支柱:
神经界面工程
微型生物传感器实时监测肠肌电活动
动态调节药物释放速率(0.05-2mg/min)
类器官预测模型
利用患者自体肠道类器官预测试验
临床疗效符合率高达91%
量子点标记追踪
精确定位药物在肠神经节的分布
避免中枢神经系统过度暴露
“这不仅是药物,更是植入体内的微型神经调节器。”研发团队透露,第二代产品已整合脑电波监测功能,可根据应激状态自动优化给药方案。
五、行业地震:从消化科到神经科的范式转移
该药物的问世正引发连锁反应:
诊断标准革新:美国胃肠病学会拟将“脑肠互动生物标志物”纳入IBS诊断指南
治疗路径重构:推荐难治性患者优先进行迷走神经功能评估
跨学科融合:神经科医生开始参与IBS多学科诊疗团队
更深远的影响体现在新药研发方向:
阿斯利康启动帕金森病肠脑轴药物研究
辉瑞布局肠源性自闭症治疗管线
六、争议与挑战:疗效背后的未解之谜
尽管前景光明,学界仍存疑虑:
长期影响:持续干预肠脑信号会否削弱神经自我调节能力。
菌群依赖性:部分患者需联合特定益生菌维持疗效。
社会公平性:年度治疗费用约7万美元,发展国内家可及性存疑。
伦理边界:健康人群能否用于预防应激性胃肠功能障碍。
欧洲药监局要求追加5年随访数据,重点监测肠神经系统自主性和认知功能变化。世界胃肠病学组织则呼吁建立全球肠脑轴药物警戒体系。
结语
当人类首次通过药理学手段修复肠脑对话,当困扰亿万患者的腹痛腹胀不再是终生诅咒,医学的边界再次被拓展。正如诺贝尔生理学奖得主Dr. James所言:“NeuroGut-1的诞生,不仅治愈了肠道,更重塑了我们对人体智慧网络的理解。”这场始于消化科的革命,或许正在揭开神经科学的新纪元。

扫一扫联系我们
获得更详细的医药咨询

扫一扫联系我们
获得更详细的医药咨询




















